EUDAMED چیست؟
فهرست مطالب:
پایگاه اطلاعاتی یکپارچه ای یا EUDAMED چیست؟
چه کسانی ملزم به ثبت در سامانه EUDAMED هستند؟
نمایندگان مجاز (Authorized Representatives ) چه کسانی هستند؟
کد شناسایی یکتای محصول (UDI) چیست؟
پایگاه اطلاعاتی EUDAMED چیست؟
با معرفی الزامات جدید MDR (EU) 2017/745 برای تجهیزات پزشکی و IVDR (EU) 2017/746 برای محصولات آزمایشگاهی، پایگاه اطلاعاتی یکپارچه ای با نام EUDAMED نیز معرفی گردید که تولید کنندگان تجهیزات پزشکی و آزمایشگاهی و کلیه شرکت های فعال در این حوزه ملزم به ثبت در این پایگاه و اخذ کد شناسه یکتا (SRN) از سوی این سایت هستند.
در واقع EUDAMED (European Database on Medical Devices) سامانه اطلاعات یکپارچه و هماهنگ اتحادیه اروپا در حوزه تجهیزات پزشکی و آزمایشگاهی است. هدف اتحادیه اروپا از ایجاد این سامانه به شرح زیر است:

-
ایجاد پایگاه واحد اطلاعاتی تجهیزات پزشکی و آزمایشگاهی کل حوزه اتحادیه اروپا
-
ارائه یک تصویر زنده از مراحل عمر یک محصول از طریق Basic UDI-DI
-
پایگاه اطلاعاتی در رابطه با تمامی شرکتهای حوزه تجهیزات پزشکی و آزمایشگاهی (Notified Body, Manufacturer, Importer, Authorized Representative and …)
-
افزایش شفافیت و دسترسی به اطلاعات در حوزه تجهیزات پزشکی و آزمایشگاهی
-
ایجاد هماهنگی بین کشورهای مختلف حوزه اتحادیه اروپا در زمینه تجهیزات پزشکی و آزمایشگاهی
چه کسانی باید در سامانه EUDAMED ثبت گردند؟
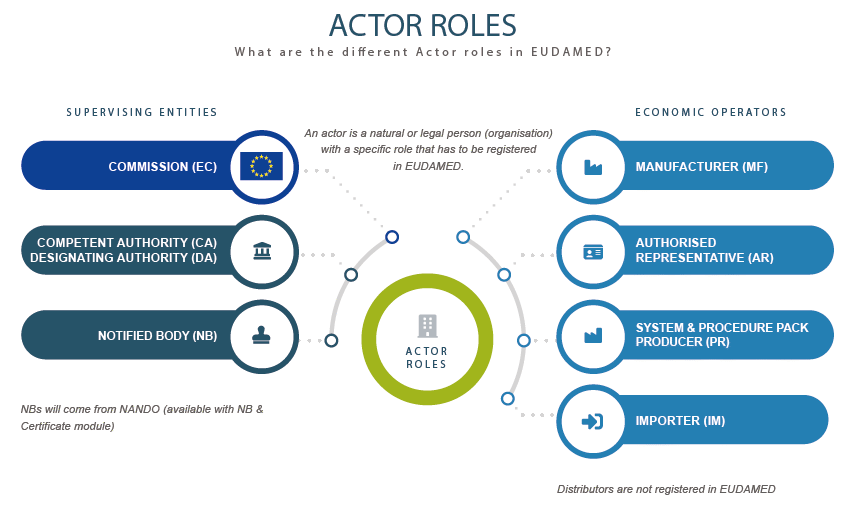
طبق الزامات جدید MDR و IVDR سه گروه ملزم به ثبت در سامانه EUDAMED هستند:
-
نمایندگان مجاز (Authorized Representatives )
-
تولید کنندگان تجهیزات پزشکی و آزمایشگاهی و بسته بندی کنندگان این تجهیزات(Manufacturers)
-
وارد کنندگان تجهیزات پزشکی و آزمایشگاهی (Importers)
به کلیه شرکتهای ثبت شده در EUDAMED، صرف نظر از نقش شرکت (تولید کننده، نماینده یا وارد کننده) یک کد منحصر به فرد (SRN: Single Registration Number) اختصاص می یابد. در نتیجه تمامی شرکتهای حوزه تجهیزات پزشکی و آزمایشگاهی که در راستای الزامات جدید MDR (EU) 2017/745 و IVDR (EU) 2017/746 قدم برداشته اند، از طریق این کد یکتا (SRN) قابل ردیابی هستند. هم چنین اطلاعاتی مانند محصولات تولید این شرکتها، کدیکتای محصولات تولیدی (Basic UDI-DI) ، کلاس خطر تجهیزات پزشکی و آزمایشگاهی، نماینده اروپایی تولیدکنندگان تجهیزات پزشکی و آزمایشگاهی و بسیاری از موارد دیگر از طریق مراجعه به سایت EUDAMED و وارد کردن کد منحصر به فرد تولید کننده(SRN) قابل دستیابی هستند.
نمایندگان مجاز (Authorized Representatives ) چه کسانی هستند؟
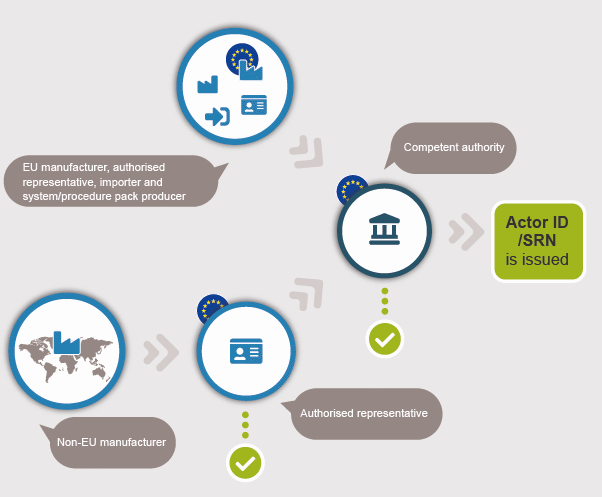
طبق الزامات جدید MDR (EU) 2017/745 و IVDR (EU) 2017/746 کلیه تولیدکنندگان مایل به فعالیت در حوزه اروپا و خواستار ثبت در پایگاه داده تجهیزات پزشکی و آزمایشگاهی اروپا (EUDAMED) که واقع در کشورهای عضو اتحادیه اروپا نیستند، ملزم هستند برای ثبت در این سامانه و صادرات محصولات خود به کشورهای اروپایی، یک شرکت واقع در خاک اتحادیه اروپا را به عنوان نماینده اروپایی خود معرفی نموده و علاوه بر اطلاعات خود، اطلاعات نماینده اروپایی انتخابی را نیز در سایت EUDAMED ثبت نمایند.
شرکت تعیین شده به عنوان نماینده اروپایی، باید به عنوان نماینده مجاز در سایت EUDAMED ثبت باشد و دارای کد شناسایی یکتا (SRN) باشد.
کد شناسایی یکتای محصول (UDI) چیست؟

دایرکتیوهای جدید MDR (EU) 2017/745 و IVDR (EU) 2017/746 تولیدکنندگان را ملزم می کند تا تمامی محصولات تجهیزات پزشکی و آزمایشگاهی خود که قصد صادرات آن به کشورهای اروپایی دارند را در پایگاه اطلاعاتی تجهیزات پزشکی و آزمایشگاهی اتحادیه اروپا یا همان سایت EUDAMED ثبت نمایند. با ثبت محصول در این سامانه، کدی منحصر به فرد (Basic UDI-DI) به محصول اختصاص می یابد.
هدف از صدور کدشناسایی منحصر به فرد (Basic UDI-DI) از سوی سایت EUDAMED برای تجهیزات پزشکی و آزمایشگاهی، بالا بردن شفافیت و میزان دسترسی به اطلاعات محصولات پزشکی و آزمایشگاهی موجود در بازار کشورهای اروپایی است. با وارد کردن کدشناسایی منحصر به فرد هر محصول ( Basic UDI-DI) اطلاعات تولیدکننده محصول و خود محصول در دسترس کاربران سایت EUDAMED قرار می گیرد؛ از این رو ثبت محصول در سایت اتحادیه اروپا (EUDAMED) و اخذ کد شناسایی یکتا برای محصول( Basic UDI-DI) فرصت مناسبی برای تولیدکنندگان تجهیزات پزشکی و آزمایشگاهی در جهت معرفی محصولات خود به بازارهای جهانی و توسعه صادرات ایجاد می نماید.

